Ricerca italiana rivela struttura tridimensionale delle metastasi mammarie e identifica possibile bersaglio terapeutico nel segnale FGF.
Per decenni lo studio del cancro si è basato su osservazioni bidimensionali: vetrini, sezioni microscopiche, immagini appiattite. Questi strumenti hanno permesso grandi progressi, ma hanno nascosto un elemento fondamentale: l’organizzazione spaziale. Oggi quella dimensione mancante è stata finalmente svelata, rivoluzionando la comprensione delle metastasi mammarie.
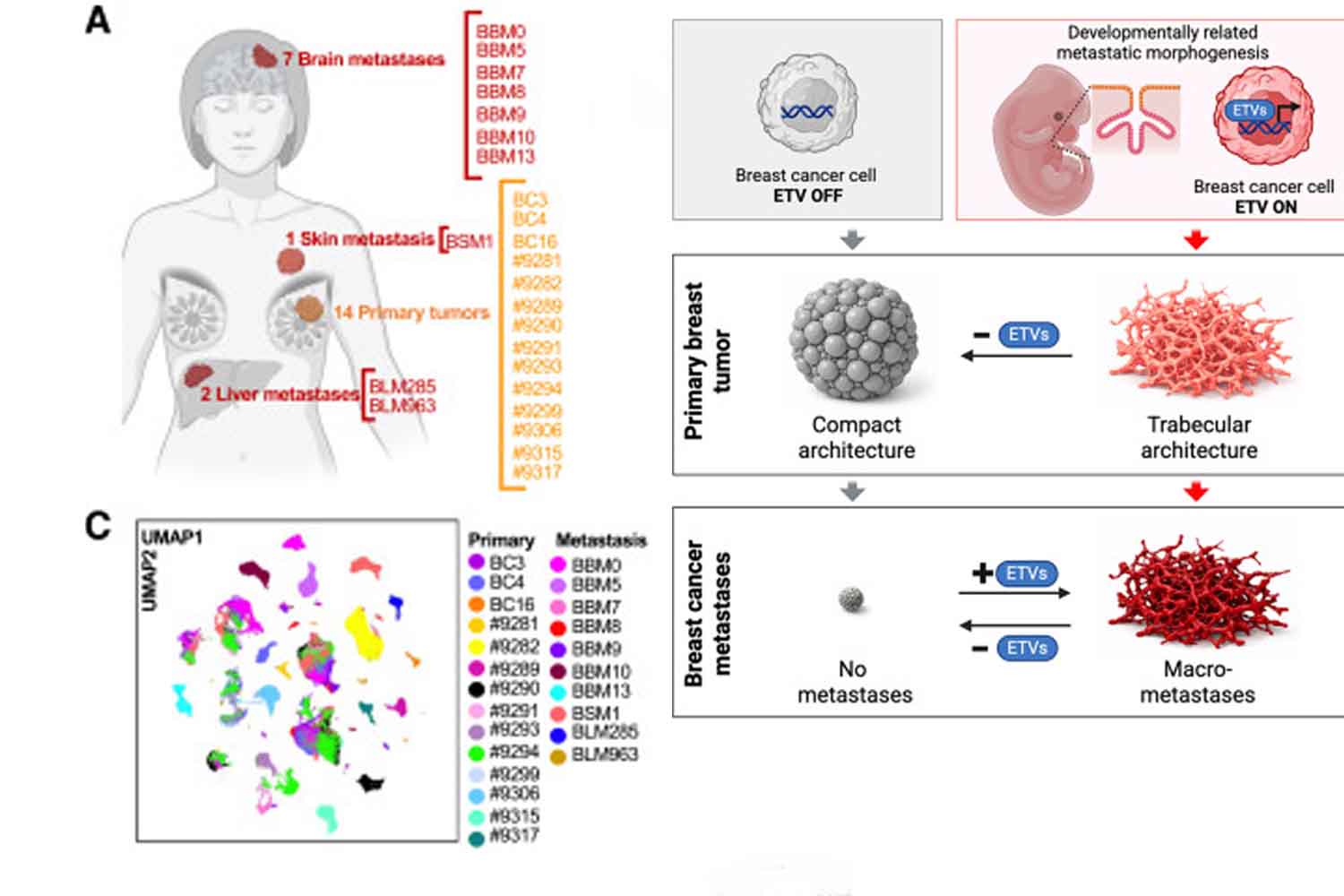
Ricercatori dell’Università di Padova, dell’Istituto Oncologico Veneto e dell’IFOM hanno presentato su Cell un lavoro che ricostruisce in tre dimensioni l’espansione metastatica, rivelando uno scenario inatteso. Non si tratta di una proliferazione caotica e disorganizzata. Al contrario, emerge un’architettura ordinata: filamenti cellulari che si estendono, si biforcano, si organizzano nello spazio secondo regole ben definite.
Questa rivelazione ha un peso enorme perché sposta il focus dalla semplice moltiplicazione cellulare all’organizzazione strutturale. Gli studiosi hanno utilizzato tecniche avanzate come il sequenziamento dell’RNA a singola cellula, la trascrittomica spaziale, l’imaging tridimensionale assistito da intelligenza artificiale e test funzionali su modelli animali per decifrare i meccanismi dell’espansione metastatica. Il risultato mostra un programma morfogenetico tridimensionale essenziale per la crescita: anziché formare ammassi compatti, le metastasi si sviluppano come reti ramificate, aperte ed estremamente efficienti nell’infiltrare i tessuti circostanti.
Secondo la ricerca, le cellule tumorali disseminate riattivano processi biologici tipici dello sviluppo embrionale, quegli stessi meccanismi che durante la formazione dell’organismo costruiscono tessuti e organi complessi. Applicata al contesto oncologico, questa capacità diventa un’arma devastante. Le metastasi mammarie, osservate da questa prospettiva, funzionano come un progetto ingegneristico biologico con regole precise, geometria definita e uso strategico dello spazio. Proprio questo aspetto rende la scoperta cruciale: dove esiste un piano costruttivo, può esistere anche una fragilità da sfruttare.
La ricerca identifica un gruppo di geni definiti “architetto”: i geni ETV. Questi regolatori orchestrano la disposizione spaziale delle cellule neoplastiche. Forniscono le istruzioni per ramificarsi, organizzarsi e assemblare la struttura tridimensionale necessaria affinché la metastasi diventi rilevabile e clinicamente significativa. Quando questi geni vengono inibiti sperimentalmente, il tumore può continuare a vivere e persino disseminarsi, ma nella maggioranza dei casi perde la capacità di costruire metastasi evidenti con quella caratteristica architettura ramificata che le rende così pericolose.
Una vulnerabilità biologica da esplorare con cautela
All’interno di questa ricerca emerge anche una potenziale direzione terapeutica, che va però interpretata con rigore scientifico e senza facili entusiasmi. Le comunicazioni ufficiali degli istituti coinvolti evidenziano come il segnale FGF, il fattore di crescita dei fibroblasti, rappresenti uno dei punti vulnerabili del meccanismo. Si tratta di una molecola fondamentale per la formazione di strutture ramificate negli esseri viventi. Secondo i dati sperimentali, bloccarne l’azione impedisce lo sviluppo metastatico lasciando sostanzialmente inalterato il tumore primario: le cellule rimangono vitali, ma perdono la capacità di edificare quella rete disseminata che caratterizza la fase più letale della malattia.
Questo risultato va comunicato con responsabilità. La ricerca traccia una pista biologica estremamente promettente, ma rimane confinata all’ambito sperimentale e preclinico. Non esistono oggi applicazioni cliniche immediate né terapie disponibili per i pazienti. Il merito sta nell’aver identificato una logica costruttiva e un possibile punto debole all’interno di quella logica. Si tratta di un avanzamento significativo per chi studia la diffusione tumorale, considerando che la fase metastatica rappresenta la sfida terapeutica più complessa e incide in modo determinante sulla mortalità. Gli stessi documenti del progetto sottolineano che circa il 90% dei decessi oncologici è attribuibile alle metastasi.
Esiste un ulteriore elemento che merita considerazione, forse ancora più rilevante dell’aspetto puramente tecnologico. Gli scienziati osservano che alcuni carcinomi mammari primari sembrano già contenere intrinsecamente questo programma di ramificazione, mentre altri ne sono sprovvisti. I tumori con struttura più ramificata risultano correlati alla propensione a metastatizzare; quelli più compatti e solidi tendono invece a comportarsi in modo più controllabile. In sostanza, il pattern di ramificazione potrebbe costituire un indicatore precoce della tendenza alla disseminazione.
Questo aspetto chiarisce perché la ricerca abbia implicazioni che vanno oltre il laboratorio. Se questa chiave interpretativa verrà confermata da studi successivi, il tumore potrà essere analizzato anche come organizzazione spaziale, non solo come insieme di alterazioni genetiche, velocità proliferativa e sensibilità ai trattamenti. Per l’oncologia significa poter discriminare con maggiore accuratezza quali lesioni possiedono realmente il programma per generare metastasi a distanza. Per i pazienti, in futuro, potrebbe tradursi in strumenti più raffinati per valutare il rischio e personalizzare le strategie terapeutiche. Attualmente rimane una prospettiva, già solida sul piano scientifico, ma ancora distante dall’applicazione clinica quotidiana.
Fonte: Cell – Università degli Studi di Padova